Der Jahresbericht der EMA mit besonderem Fokus auf: Krebsmedikamente, datengesteuerte Arzneimittelregulierung sowie Transparenz und Kommunikation. (Foto Screenshot Website / PM—Report)
Im Bericht sind außerdem eine Auswahl wichtiger Zahlen und interessanter Trends enthalten, die die Arbeit der EMA aufzeigen sollen.
Einige Ergebnisse in der Übersicht:
- Im Jahr 2023 empfahl die EMA die Zulassung von 77 Humanarzneimitteln, darunter 39 mit einem neuen Wirkstoff.
- Viele dieser Behandlungen stellten in ihren Therapiebereichen bedeutende Fortschritte dar.
- Zwei Impfstoffe zum Schutz vor Erkrankungen der unteren Atemwege, die durch das Respiratorische Synzytialvirus (RSV) verursacht werden, erhielten vom Ausschuss für Humanarzneimittel (CHMP) der EMA eine positive Stellungnahme zur Zulassung in der EU.
- Die EMA empfahl auch die Zulassung des ersten Arzneimittels für neuartige Therapien, das die bahnbrechende Gen-Editierungstechnologie CRISPR/Cas9 zur Behandlung von zwei seltenen Bluterkrankungen (Beta-Thalassämie und schwere Sichelzellenanämie) verwendet.
- Darüber hinaus verabschiedete die Agentur zwei positive Stellungnahmen für Arzneimittel zur Verwendung in Ländern außerhalb der EU.
- Im Bereich der Tierarzneimittel empfahl die EMA 14 Arzneimittel zur Marktzulassung.
- Davon hatten neun einen neuen Wirkstoff – eine Verdreifachung im Vergleich zu 2022.
- Neun waren Impfstoffe, darunter sechs neue biotechnologische Impfstoffe.
- Im Jahr 2023 startete die Agentur eine neue Initiative namens „Cancer Medicines Pathfinder“, um die Entwicklung und Zulassung von Krebsmedikamenten, die einen bedeutenden Einfluss auf die Patientenversorgung haben könnten, weiter zu unterstützen. Diese Initiative untersucht, wie die EMA die Arzneimittelbewertung insgesamt verbessern kann, indem sie die Erkenntnisse aus der COVID-19-Pandemie anwendet.
- Der Bericht beschreibt die Fortschritte mit dem Cancer Medicines Pathfinder und seinen drei Säulen: Beschleunigung der Arzneimittelbewertungen, Stärkung des Dialogs mit Interessengruppen und Kommunikation von Nutzen und Risiken.
Zu verstehen, wie Daten effizient analysiert und genutzt werden können, um die Arzneimittelregulierung zu informieren, war für die Agentur und das europäische Arzneimittelregulierungsnetzwerk im Jahr 2023 eine wichtige Priorität. Denn „es ist wichtig sicherzustellen, dass das EU-Regulierungssystem das volle Potenzial der Daten ausschöpfen kann“, schreibt die EMA.
Der Aufbau von Vertrauen in die Arzneimittelregulierung durch Transparenz und Kommunikation ist ebenfalls eine wichtige Priorität für die EMA. Der Bericht erklärt deswegen auch die Maßnahmen, den europäischen Bürgern über die Website der EMA, Social-Media-Kanäle und traditionelle Medien „zeitnahe, genaue und umfassende Informationen zu Arzneimitteln bereitzustellen.“
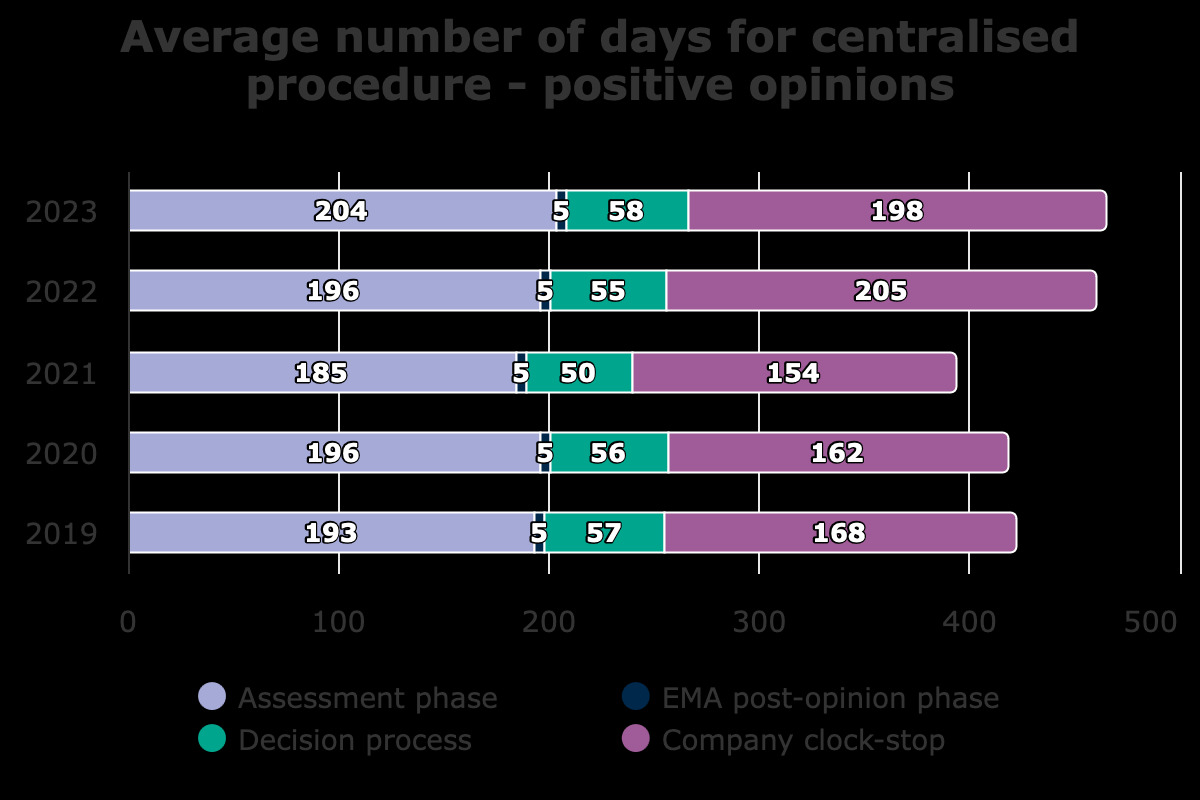
Grafik: EMA

Grafik: EMA
Erhalten Sie jetzt uneingeschränkten Zugriff auf alle interessanten Artikel.
- Online-Zugriff auf das PM-Report Heftarchiv
- Aktuelle News zu Gesundheitspolitik, Pharmamarketing und alle relevanten Themen
- 11 Ausgaben des PM-Report pro Jahr inkl. Specials

